세부 콘텐츠 상세
목록
- 등록자
박지은
- 등록일
2025-07-31
- 조회수
978
초소형 유전자가위 치료제를 꿈꾸다
아픔을 희망으로 교정하는 ‘진코어’
기존 유전자가위 크기 문제를 해결할 초소형 유전자가위 기술 개발
헌팅턴병, 루게릭병 등 뇌유전질환 대상 치료제개발 집중
한국생명공학연구원 연구소 창업 신화 이어가

한국생명공학연구원에서 유전자교정 분야 연구를 이어오다 초소형 유전자가위 기술로 창업을 결심한 김용삼 진코어 대표.
지난 2012년 에마뉘엘 샤르팡티에(Emmanuelle Marie Charpentier) 박사와 제니퍼 다우드나(Jennifer Anne Doudna) 교수 공동연구팀은 crRNA의 염기서열을 일부 바꿔 유전체를 교정할 수 있는 ‘유전자가위’ 논문을 발표했다. 해당 논문은 당시 과학기술계에 충격을 안겨주었고, 채 10년이 지나지 않은 2020년에는 노벨화학상을 두 과학자에게 안겨주었다.
전 세계가 유전자가위 개발 경쟁에 뛰어들었고, 지난 2023년 12월 최초의 유전자가위 치료제 ‘카스거비(Casgevy)’가 세상에 등장했다. 과거 공상과학소설과 영화 속에서만 가능하다고 여겨졌던 기술은 더 이상 상상 속의 기술이 아니게 된 것이다.
이 가운데 기존 알려진 유전자가위보다 더 작은 ‘초소형 유전자가위’로 유전자치료제 시장의 새로운 혁신을 준비하는 대전의 바이오헬스 기업이 있다. 한국생명공학연구원의 연구소창업 기업이자 핵심유망으로 꼽히는 진코어(대표 김용삼)가 그 주인공이다. 이번 D-Special에선 유전자치료제를 통해 인류의 건강한 삶을 꿈꾸는 진코어의 이야기를 소개한다.
◆ 고세균에서 찾은 초소형 유전자가위···인체 구석구석 치료물질 전달
“데이터가 읽기만 가능했던 시절에서 쓰기가 가능해짐에 따라 IT산업의 새로운 시대가 열렸듯이, 유전자 역시 그동안 염기서열을 읽기만 했던 수준을 넘어 교정이 가능해졌다는 점에서 앞으로 새로운 혁신들이 이어질 것으로 기대합니다.”
김용삼 대표는 한국생명공학연구원 유전자교정센터 센터장, 한국유전자교정학회 회장 등을 역임한 국내 유전자교정분야 전문가다. 유전자교정 기술을 연구하던 그에게 유전자가위의 등장은 누구보다 반가운 소식이었다. 특히나 유전자교정을 통한 유전질환 치료의 다양한 가능성이 열리게 된 가운데, 그는 기존 기술의 단점을 보완해줄 수 있는 초소형 유전자가위 기술을 활용한 창업을 결심했다.
진코어의 핵심이 되는 초소형 유전자가위는 말 그대로 크기가 작다는 특징이 있다. 작은 크기가 갖는 이점은 전달체에 있다. 유전자가위 치료제는 특정 유전질환에 작용하는 유전자가위를 전달체에 넣어 인체에 투여한다. 이렇게 투여된 치료제는 뇌, 심장, 폐, 간 등과 같이 해당 유전질환이 발생한 곳으로 이동해 문제가 되는 염기서열을 교정하는 과정을 거친다.
현재 크리스퍼(CRISPR-Cas9) 전달체로 주로 사용되는 지질 나노 입자(Lipid Nanoparticle, LNP)는 간에는 전달이 잘 된다는 장점이 있지만, 이외의 장기에는 전달력이 떨어지는 상황이다.
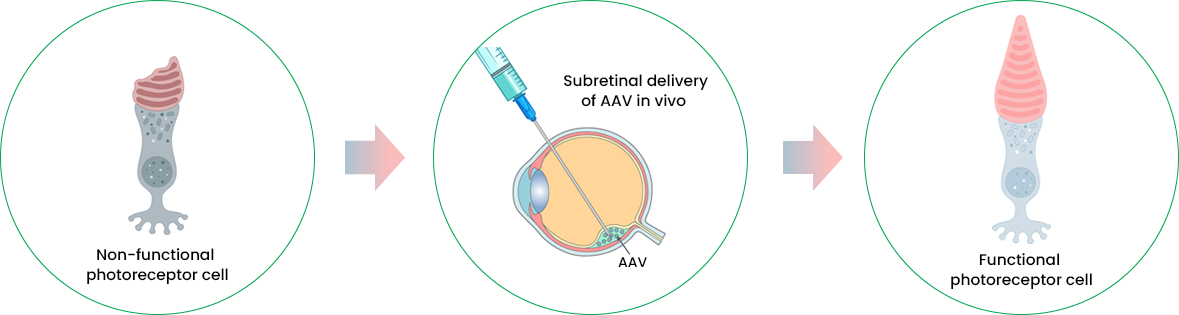
아데노연관바이러스(AAV)를 전달체로 삼아 초소형 유전자가위 치료제를 망막세포에 전달해 시각장애를 치료하는 기술.[사진=진코어 제공]
또 다른 전달체로는 바이러스 벡터를 기반으로 한 전달체다. 그 중 가장 보편적으로 사용되는 아데노연관바이러스(AAV)는 자연계에 여러 타입이 존재하기 때문에 특정 타깃에 맞는 전달체를 확보할 수 있다는 것이 장점이다. 그러나 바이러스 자체가 크기가 작다 보니 크리스퍼 유전자가위 자체를 바이러스 안에 넣지 못한다는 단점이 있다.
즉, 바이러스 전달체에 유전자가위를 담기 위해선 유전자가위 자체를 작게 만들어야 했다. 해답은 고세균에 있었다. 김 대표는 “크리스퍼는 본래 세균에서 발견된 유전자가위다. 세균 역시 진화를 해오며 크기가 커졌기 때문에 그 안에 있던 크리스퍼 역시 자연스럽게 크기가 컸다”며 “심해, 화산, 유황온천 등 극한 환경에 분포하는 고세균과 같은 미생물에서 크기가 작은 크리스퍼를 확보할 수 있었으며, 이를 유전자가위 치료제로 활용했다”고 설명했다.
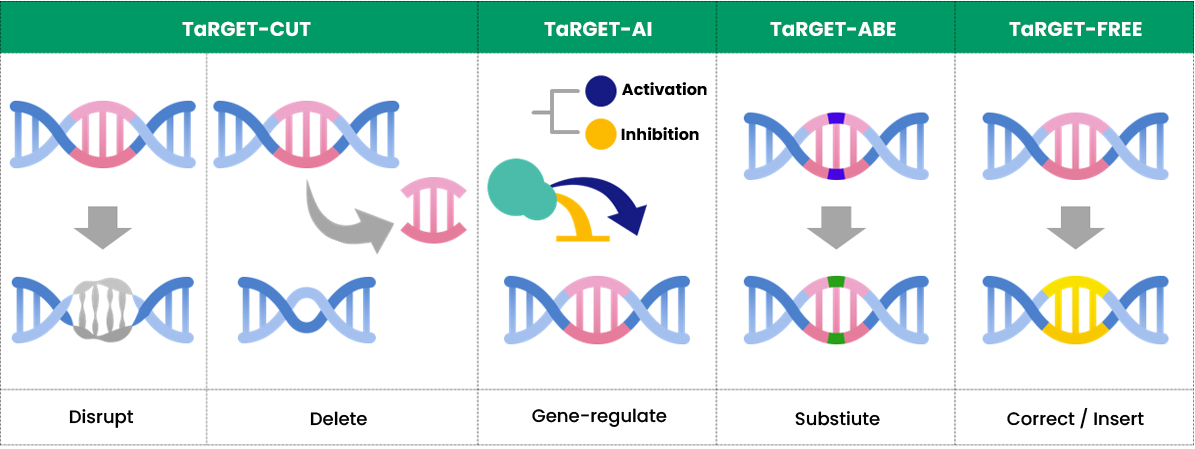
초소형 유전자가위를 통해 유전자를 자르거나 교체, 삽입할 수 있다.[사진=진코어 제공]
물론 초소형 유전자가위가 만능인 것은 아니다. 세균과 크리스퍼는 인간과 같은 환경에서 진화해왔다. 때문에 이를 활용한 치료제를 인간에 투여하더라도 면역거부 및 독성 반응이 낮다. 그러나 고세균의 경우 안정성과 효율면에서 부족한 부분들이 있다.
김 대표는 “현재 헌팅턴병, 뇌전증, 루게릭병 등 뇌질환을 타깃으로 동물실험을 진행하며 유효성 테스트를 진행하고 있다. 향후엔 북미 지역의 임상을 계획하고 있다”며 “뇌질환 자체가 어려운 분야이지만 도전적인 연구개발을 통해 혁신신약개발에 도전할 것”이라고 말했다.
◆ 국가전략기술 확인 받은 기술력, 뇌유전질환 치료 가능성 높인다
대전광역시의 주요 전략산업 중 바이오헬스 분야는 민간주도의 클러스터라는 독특한 경쟁력을 갖고 있다. 과거 한국생명공학연구원과 LG생명과학 출신 연구자들의 벤처창업이 활발하게 이뤄졌고, 우수한 기술력을 바탕으로 현재 글로벌 시장과 코스닥 시장에서 뛰어난 경쟁력을 보여주고 있다. 또한 자체적인 커뮤니티를 구성하고 지속적인 네트워킹을 통해 시너지를 보이고 있으며, 신진 후배 기업들의 성장에도 도움을 주고 있다.
진코어 역시 한국생명공학연구원 출신의 김 대표의 기술력이 빛나는 기업이다. 진코어는 현재 한국생명공학연구원 내에 둥지를 틀고 있으며, 지속적인 연구협력을 통해 그 경쟁력을 강화하고 있다.

김용삼 대표는 초소형 유전자가위 치료제로 환자들의 건강한 삶에 기여함은 물론, 전 세계로 진코어의 이름을 알려나가겠다는 뜻을 밝혔다.
물론 상대적으로 아쉬운 점도 있다. 김 대표는 “국내 유수의 연구기관, 그리고 KAIST가 바로 옆에 있지만 바이오헬스 분야 특성상 임상을 진행할 대형병원의 선택지가 적다”며 “또한 인력 채용에 있어 수도권과의 경쟁에서 어려움을 겪는다”고 말했다. 진코어는 이를 부분적으로 해소하기 위해 가톨릭중앙의료원 옴니버스파크에 서울연구센터를 마련했다. 서울의 연구인력 채용과 함께 가톨릭대학교 서울성모병원과의 협력도 이어가고 있다.
진코어의 기술력은 투자유치 및 성과에서도 확인할 수 있다. 2019년 창업당시 36억 원 규모의 시드투자와 2020년 171억 원 규모의 시리즈A, 2025년 100억 원 규모의 브릿지 펀딩까지 순차적인 투자유치를 이어왔다. 2023년 1월 미국 글로벌 제약사에 4,500억 원 규모의 대형 기술이전 계약도 체결했다. 또한 2024년 12월에는 진코어의 초소형 유전자가위 기술이 ‘국가전략기술’로 확인받으며 향후 상장과정에서의 우대혜택도 받게될 예정이다.
김 대표는 “유전자가위 기술이 상용화까지는 조금 거리가 있다 보니 최근 관심이 조금 사그라든 감이 있지만, 진코어만의 페이스로 지속적인 기술 고도화를 이어나갈 계획이다”라며 “새로운 유전자가위 치료제의 데뷔를 통해 진코어의 이름을 알리고, 환자분들의 건강한 삶에 기여할 수 있도록 노력하겠다”는 뜻을 밝혔다.